代謝相關新microRNA——miR-378a
代謝性疾病,如2型糖尿病或肥胖癥,是機體代謝途徑中斷的結果。小非編碼RNA——microRNAs(MiRNAs)——作為轉錄后基因調節因子的發現,為開發新的策略來對抗上述疾病打開了新的大門。miR-378a,miR-378a-3p和miR-378a-5p的兩條鏈在Ppargc1b基因中編碼,在如線粒體代謝和自噬等幾種代謝途徑的調節中起著積極的作用。最近的研究確認miR-378a是能量和葡萄糖穩態的重要調節因子,并強調它是改善代謝失調的潛在靶點。在綜述“miR?378a: a new emerging microRNA in metabolism”中,討論了miR-378a的已有知識,并特別強調其在新陳代謝、線粒體和自噬中的生物學功能和作用機制。

一、miR-37a對代謝的調節
1.miR-378a的起源和結構
過氧化物酶體增殖物激活受體-γ(PPARγ)協同激活因子-1β(PGC-1β)由基因Ppargc1b編碼并在其第一內含子中嵌入miR-378家族的兩個成員(圖1)。
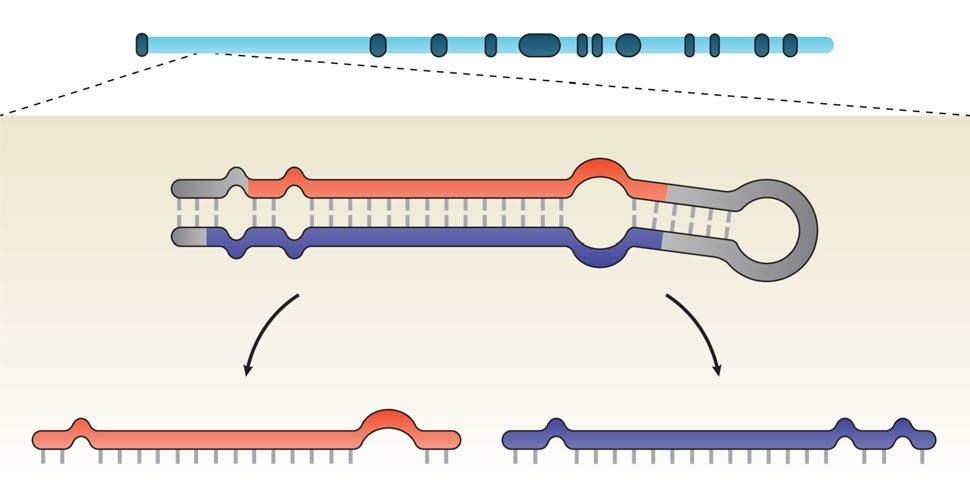
圖一:miR-378a在Ppargc1b中的基因組定位。MIR-378a位于Ppargc1b的第一內含子中,其preRNA的加工產生了兩條鏈,miR-378a-5p和miR-378a-3p。miR-378a-3p:通常被識別為miR-378,曾被命名為miR-422b。miR-378a-5p:通常識別為miR-378*。miR-378a-3p和miR-378a-5p在線粒體豐富的組織中表達,如骨骼肌、心臟、肝臟和棕色脂肪組織(BAT),且可能參與PGC-1β調控的代謝途徑,如葡萄糖和系統能量穩態、脂肪酸氧化和線粒體代謝。此外,這些miRNAs還與癌癥代謝和組織分化有關,例如,miR-378a通過抑制肌源性抑制因子MyoR誘導成肌細胞分化,對牛前脂肪細胞誘導分化,通過下調MAPK1誘導3T3-L1細胞分化,在棕色脂肪細胞分化過程中觀察到miR-378a-3p水平升高,與先前觀察到的PGC-1βmRNA水平在BAT分化和C2C12成肌細胞分化過程中升高的情況一致。
2. miR-378a在腫瘤發展中的作用
瓦爾堡效應是指在有氧條件下,癌細胞優先選擇糖酵解而不是氧化磷酸化作為其主要的能量代謝途徑,其主要目的是通過將糖酵解中間體引導到生物合成途徑中來促進癌細胞的增殖和生長。但癌細胞的新陳代謝是收多種因素調節的,如miRNAs。
已有報道miR-378a參與腫瘤代謝、腫瘤生長和血管生成。miR-378a-5p的過度表達導致雌激素相關受體γ(ERRγ)和轉錄因子GA結合蛋白α(GABA PA)的mRNA水平降低,揭示了內含子miRNA直接參與其宿主基因伙伴的調節。MIR-378a-5p也被發現是乳腺癌細胞中瓦爾吧效應的主要參與者。它的過度表達有利于糖酵解途徑,通過下調編碼三羧酸(TCA)循環的代謝物的代謝基因,ERRγ靶向,同時減少有氧呼吸。
3. miR-378a在代謝失調中的作用
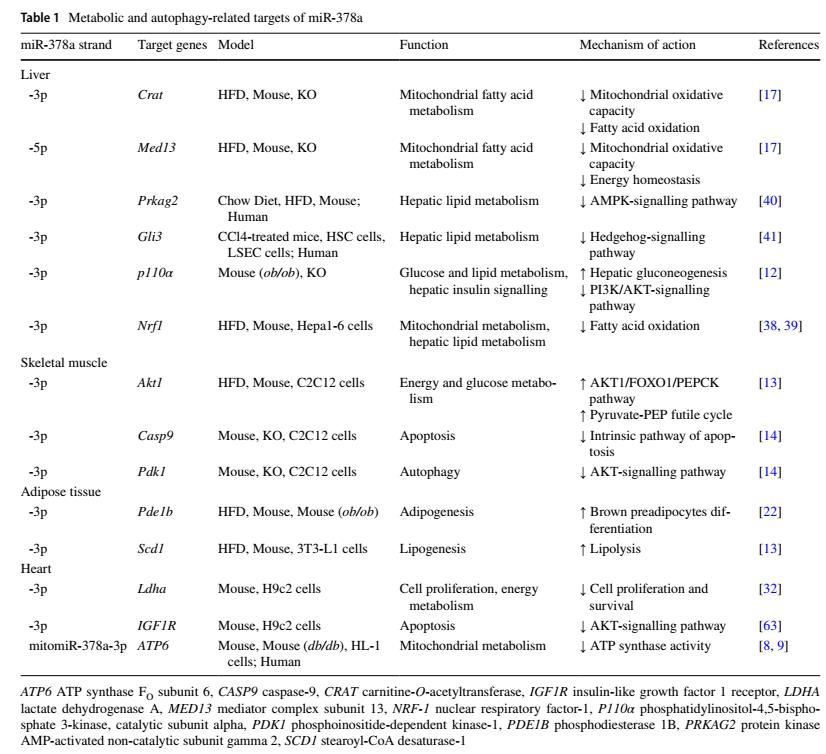
miR-378a-3p和miR-378a-5p參與了代謝紊亂的調控,被發現可干擾大量的細胞過程(表1)。
表一 miR-378a的代謝和自噬相關靶點
有研究報道,絲氨酸/蘇氨酸蛋白激酶(SRPK1)的減少和增加都會通過激活AKT導致相同的致瘤表型,miR-378a對新陳代謝的調節也可能存在類似的機制。此外, miR-378a-3p在小鼠中的過表達導致骨骼肌無用循環的激活,同時改善脂肪組織中的脂解作用。進一步的實驗發現Akt1是miR-378a-3p的主要靶標,被發現通過AKT1/FOXO1/PEPCK途徑激活PEP-磷酸烯醇式PEP無效循環(圖2A)。PEP可以直接還原為乳酸,而不是用于為無效循環提供燃料; miR-378a-3p過表達不影響乳酸水平或乳酸脫氫酶A(LDHA)轉錄本水平。
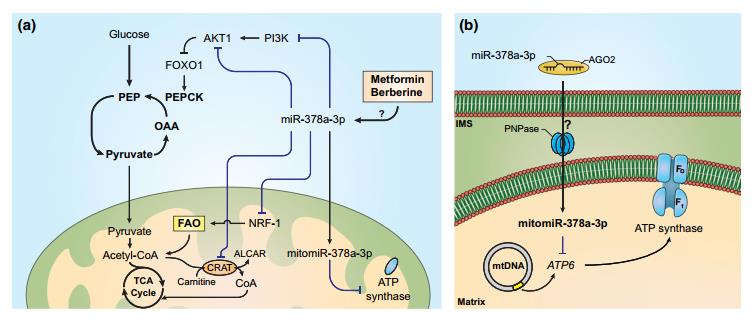
圖二 miR-378a-3p對代謝和線粒體途徑的調節。a miR-378a-3p在調節氧化和線粒體代謝中起著至關重要的作用,被發現能抑制胰島素途徑的重要元件PI3K和AKT1。此外,抑制AKT1刺激了骨骼肌中的Pyruvic Acid-PEP無效循環。此外,miR-378a-3p抑制了氧化代謝的關鍵調節因子,如NRF-1和CRAT。b miR-378a-3p轉運到線粒體的模型,在其中干擾線粒體基因的轉錄,如ATP6。另一項研究報道miR-378a-3p靶向并能夠抑制H9c2心肌細胞中的LDHA。miR-378a-3p導致葡萄糖代謝中斷,導致骨骼肌的能量缺乏狀態,這被證明是獨立于胰島素信號傳導的。
4. miR-378a在線粒體功能障礙中的新作用
線粒體功能障礙是一些代謝性疾病的特征。miR-378a參與線粒體內氧化代謝的調控,其抑制作用被證明改善線粒體的氧化能力并增加了耗氧量;miR-378a-3p針對核呼吸因子-1(NRF-1);miR-378a-3p在HFD喂養的小鼠肝臟中上調,抑制NRF-1,導致肝臟骨質疏松癥的惡化。miR-378a-3p的過度表達抑制Nrf1促進脂質積累和損害脂肪酸氧化,導致肝骨病的加重(圖2A)。此外,NRF-1和miR-378a-3p似乎參與了前饋環,其中NRF-1轉錄抑制miRNA。miR-378a-3p還被報道是一種在HFD處理的小鼠肝臟中通過靶向其編碼基因Prkag2的亞基AMPKγ2的抑制劑。miR-378a-3p似乎在纖維化中具有雙重作用,它有利于肥胖小鼠的肝纖維化,而當在有肝纖維化的動物身上使用時則具有治療作用。
1)線粒體基因組的調節因子mitomiR?378a?3p
成熟的miRNAs高度集中在細胞質中,但它們在細胞核或線粒體等細胞器中亦有存在。有報道稱功能性miRNAs位于線粒體內,被命名為線粒體定位miRNAs(MitomiRs),并被證明在線粒體基因表達調控中具有積極作用。事實上,線粒體可以由能夠干擾線粒體DNA轉錄的mRNA的有絲分裂因子進行內部調節。miR-378a-3p被鑒定為mitomiR(mitomiR-378a-3p),并被發現干擾編碼ATP合成酶FO亞單位6的線粒體ATP6。
2)復合物I抑制劑調節miR - 378a的表達
線粒體復合物I是組成電子傳遞鏈的主要復合物之一,使其成為干擾氧化磷酸化的合適靶標。melbine是治療T2 DM的常用雙胍類藥物,可抑制肝臟糖異生,繼而導致肝臟葡萄糖生成減少。melbine通過特異性抑制呼吸鏈復合物I而發揮作用,導致細胞內AMP/ATP比值升高,從而觸發AMPK及其相關信號通路的激活。isoquinoline生物堿小檗堿也被報道分別通過抑制復合物I和通過激活骨骼肌和肝臟中的SIRT1和SIRT3激活AMPKor來改善T2 DM的狀況。這兩種抗糖尿病化合物被證明參與了miRNAs的調節。使用鎖定核酸(LNA)技術的miRNA圖譜顯示,在MIHA和HepG2細胞中,小檗堿處理似乎誘導了miR-378a的表達。此外,有報道melbine能夠提高miR-378a-3p的表達水平。miR-378a-3p被證明是通過靶向細胞周期依賴性激酶1(CDK1)并下調這一重要的細胞分裂因子而抑制肝癌細胞增殖的重要角色,進而導致抑制腫瘤生長。這是一個值得注意的發現,因為miR-378a-3p刺激肝糖異生基因的表達,而melbine已知可以抑制肝糖異生。因此,這個問題需要進一步闡明,以了解melbine是如何上調miR-378a-3p的,以及它在多大程度上參與了melbine的作用機制。
5. miR - 378a可調節內分泌
一些細胞外miRNAs存在于血漿和血清中,甚至在健康和患病個體中表達不同。這表明miRNAs作為內分泌分子能夠調節遠距離靶細胞的基因表達,還可以作為疾病生物標記物的潛在用途。一些研究已經提供了證據支持細胞外miRNAs在癌癥、心血管疾病或代謝性疾病中的生物學功能。最近的研究報道,在生物體液中發現miR-378a和其他幾種miRNAs。例如,與1型糖尿病和中度DKD患者相比,miR-378a-5p在重度糖尿病腎病(DKD)患者的外周血液中上調。在未來,確定這些修飾是否是組織特異性的,或者它們是否是從循環中攝取miRNA并從組織中釋放的結果是至關重要的。現有的研究主要集中在對某一疾病中大量的胞外miRNAs的評價,而沒有對胞外miR-378a的生理功能進行詳細的探討。因此,有關miR-378a內分泌功能的一些重要問題仍需進一步探討。
二、miR - 378a對程序性細胞死亡的調節作用
細胞存在多種死亡機制:凋亡、自噬或壞死。近年來,已發現miRNAs與自噬相關,可干擾宏觀自噬途徑不同階段的組分。miR-378a可以調節細胞凋亡和自噬,有報道稱轉染miR-378a-3p的缺氧H9c2細胞通過降低CASP3蛋白水平而抑制凋亡并提高細胞存活率,而miR-378a-3p抑制則加劇了凋亡。胰島素樣生長因子1受體(IGF1R)被鑒定為miR-378a-3p的直接靶標,抑制AKT信號傳導,從而導致促凋亡蛋白的上調,促進細胞死亡。
miR-378a在宏觀自噬中的作用亦已被驗證。miR-378a-3p對于維持骨骼肌細胞凋亡和自噬等細胞死亡程序是重要的。miR-378a在禁食或饑餓應激下上調,并被炎癥抑制。miR-378a-3p通過抑制CASP9抑制凋亡,并通過靶向和抑制正常激活AKT的磷酸肌醇依賴性激酶-1(PDK1)來增強宏觀自噬。宏觀自噬可由三個與AKT相互作用的不同因子調節:FOXO1,FOXO3和哺乳動物靶標雷帕霉素復合物1(MTORC1)。一方面,miR-378a-3p導致FOXO1和FOXO3的激活,正向調節宏觀自噬。另一方面,mTORC1因此被miRNA抑制,導致自噬誘導劑ULK1復合物的激活。此外,缺乏miR-378a-3p/miR-378a-5p的小鼠在腓腸肌中發現異常腫脹的線粒體堆積。評估線粒體功能以進一步證實線粒體氧化代謝受到miR-378a缺失的負面影響是很有意義的。






