LncRNA MILIP促進透明細胞腎細胞癌的轉移
遠處轉移是透明細胞腎細胞癌(ccRCC)相關死亡率的主要原因。然而,涉及ccRCC轉移的分子機制仍有待充分了解。隨著lncRNAs在癌癥發展、進展和治療耐藥性中的作用越來越被重視,導致ccRCC發病機制的異常表達lncRNAs的列表正在迅速擴大。與原發ccRCC組織相比,轉移性ccRCC中MILIP表達上調。轉移性ccRCC細胞中MILIP表達增加是由TFAP2C驅動的。MILIP的敲低降低了ccRCC細胞在體外遷移和侵襲的潛能,并減少了ccRCC在體內轉移病灶的形成。MILIP對ccRCC細胞的影響與EMT標志基因表達的改變有關。機制上,MILIP與Snai1 mRNA形成RNA-RNA雙鏈,并與YBX1結合。這促進了YBX1蛋白和Snai1 mRNA之間的關聯,導致后者的翻譯增加。Snai1反過來在MILIP驅動的ccRCC轉移中發揮重要作用。總之,TFAP2C響應的lncRNA MILIP驅動ccRCC轉移。因此,靶向MILIP可能是ccRCC治療的潛在途徑。本文于2022年8月發表于Journal of Experimental & Clinical Cancer Research ( IF=12.658 )上。
技術路線

結果
1)TFAP2C驅動轉移性ccRCCs中上調的MILIP表達
通過查詢ccRCC數據集(GSE22541),我們發現,與原發腫瘤相比,轉移病灶來源的ccRCC組織中lncRNA MILIP表達水平更高(圖1a)。此外,MILIP高表達與ccRCC患者無病生存期(DFS)較差相關(圖1b)。對CCLE的ccRCC細胞系數據集的分析顯示,與原發腫瘤相比,轉移性腫瘤產生的ccRCC細胞系中MILIP表達水平更高(圖1c)。我們證實,在FFPE ccRCC樣本隊列中,與原發性ccRCC樣本相比,轉移性ccRCC中MILIP表達增加(圖1d, e)。類似地,MILIP表達水平在轉移性細胞系中更高(cki -1和ACHN) (圖1f)。接著,為了了解在ccRCC細胞中調控MILIP表達的轉錄機制,我們使用生物信息學查詢其啟動子的轉錄因子結合位點。這揭示了位于 MILIP 基因啟動子-837/-847 區域的轉錄因子 TFAP2C 的共有結合基序(圖1g)。來自ENCODE的ChIP-seq數據分析顯示,在TFAP2C結合區(TFAP2C-BR)有一個TFAP2C結合峰(圖1g)。該區域與內源性TFAP2C共同沉淀,是MILIP轉錄上調所必需的(圖1h, i)。此外,TFAP2C的敲除降低了Caki-1和ACHN細胞中MILIP的轉錄活性(圖1j),支持MILIP 通過已識別的 TFAP2C-BR 被 TFAP2C 轉錄激活。為了證實這一點,TFAP2C的敲除降低了內源性MILIP水平(圖1k)。此外,與MILIP的高表達一樣,在GSE22541數據集中,TFAP2C的高表達與ccRCC患者較差的DFS相關(圖1l)。通過qPCR分析和原位雜交(ISH)分析顯示,MILIP主要位于ccRCC細胞的細胞質中(圖1m, n)。
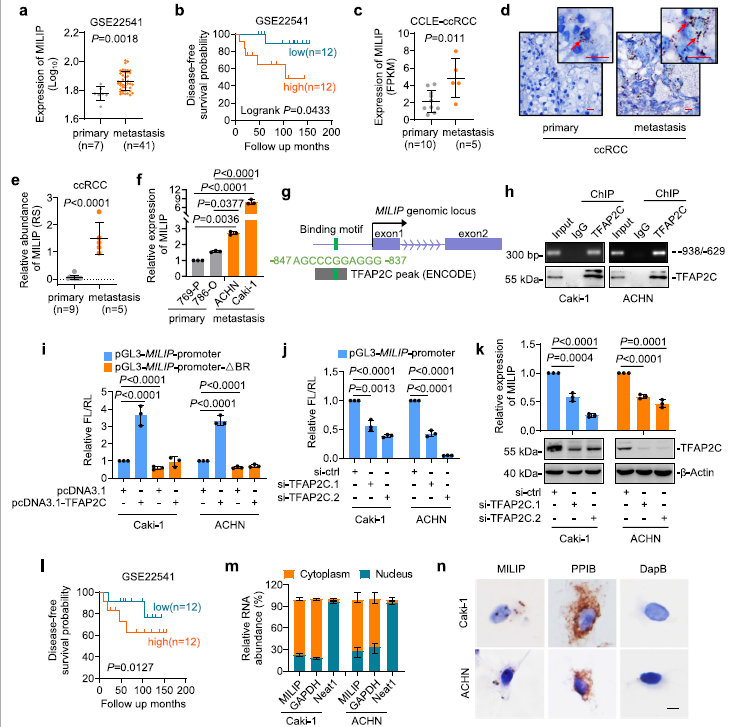
2)MILIP促進ccRCC轉移
在發現MILIP在轉移性ccRCC中特異性上調后,我們重點研究了MILIP對ccRCC細胞侵襲和轉移的潛在作用。MILIP的敲除在劃痕試驗中顯著延遲了Caki-1和ACHN細胞的傷口愈合,并在transwell試驗中減少了它們的遷移和侵襲(圖2a-e)。來自Caki-1細胞的RNA測序數據的GSEA顯示MILIP敲除導致轉移途徑基因特征的減少(圖2f)。此外,MILIP的敲低導致上皮標記物E-cadherin的上調以及間充質標記物N-cadherin、MMP2和波形蛋白的下調,而MILIP過表達導致E-cadherin的降低,N-cadherin、MMP2和波形蛋白的表達上調(圖2g,h)。此外,shMILIP細胞顯著減少了肺轉移病灶的形成(圖2i-l)。總之,這些結果表明MILIP促進ccRCC細胞的細胞侵襲和遷移,這與增強EMT有關。
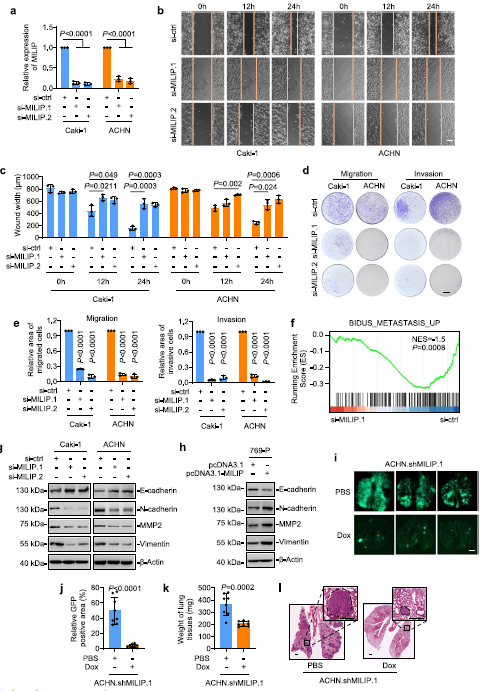
3)MILIP與YBX1相互作用,促進Snai1的翻譯激活
為了了解ccRCC細胞中MILIP介導的EMT促進機制,我們使用RNA下拉和質譜分析確定了與MILIP相互作用的蛋白質。與MILIP共沉淀的最豐富的蛋白質是YBX1(圖3a),這是一種核酸結合蛋白,已知可翻譯激活Snai1,通過轉錄抑制下調E-cadherin表達,從而促進EMT。在Caki-1和ACHN細胞中使用RNA下拉和RIP測定確認了MILIP和YBX1之間的關聯(圖3b,c)。為了確定負責與YBX1相互作用的MILIP區域,我們對體外轉錄的MILIP突變體進行了映射實驗。該分析表明,位于外顯子2 (E2)內的MILIP片段618-989是其與YBX1結合的關鍵(圖3d)。另一方面,YBX1的CSD缺失減少了其與MILIP的關聯(圖3e)。值得注意的是,MILIP的敲低導致Snai1蛋白水平的下調,而不影響Snai1 mRNA表達(圖3f)。環己酰亞胺追蹤實驗表明,MILIP的敲除不會改變Snai1蛋白的周轉率(圖3g,h)。Snai1的敲低消除了MILIP過表達誘導的ccRCC細胞遷移和侵襲(圖3i,j),表明Snai1對于MILIP介導的ccRCC細胞轉移的促進至關重要。
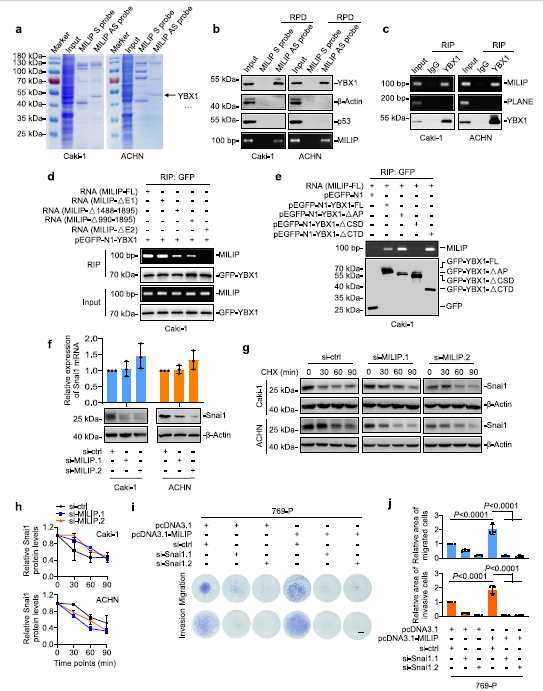
4)MILIP與Snai1 mRNA形成RNA-RNA雙鏈
我們研究了MILIP如何促進Snai1的翻譯激活。使用IntaRNA程序進行的生物信息學分析確定了Snai1 mRNA的5′UTR附近的潛在MILIP結合區(MILIP-BR),該區域與MILIP中富含 DFO的片段互補。體外合成的生物素標記的MILIP RNA沉淀了含有MILIP-BR的RNA片段(圖4a)。然而,當MILIP內富含DFO的片段被刪除時,這種關聯性減弱(圖4a)。因此,MILIP和Snai1 mRNA分別通過DFO和MILIP-BR形成RNA-RNA雙鏈體。作為支持,內源性MILIP從Caki-1和ACHN細胞提取物中沉淀Snai1 mRNA(圖4b)。我們還測試了RNA-RNA雙鏈在MILIP介導的Snai1翻譯調控中的功能重要性。與野生型MILIP的過表達(圖4c)相反,將缺乏DFO的MILIP突變體(MILIP-ΔDFO)轉染769-P細胞不會影響Snai1蛋白表達水平,也不會影響細胞遷移和侵襲(圖4c-e)。因此,RNA-RNA雙鏈的形成是MILIP介導的Snai1翻譯促進所必需的。
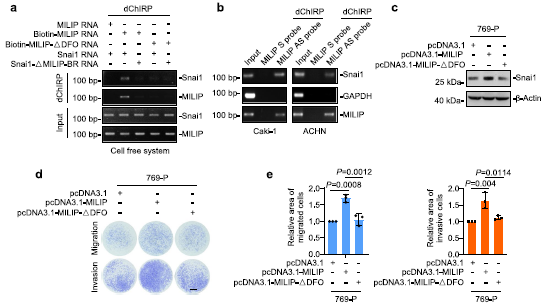
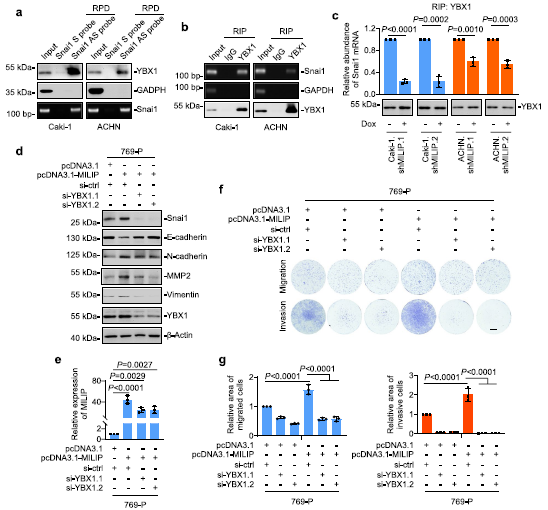
我們接下來研究了MILIP和YBX1在調節Snai1 mRNA翻譯中的關系。正如預期的那樣,YBX1與Snai1 mRNA結合(圖5a,b)。然而,在MILIP敲低的細胞中,YBX1和Snai1 mRNA之間的這種關聯減少(圖5c),表明MILIP促進YBX1與Snai1 mRNA的關聯。一致地,在769-P細胞中,YBX1的敲除消除了MILIP過表達觸發的Snai1、N-cadherin、MMP2和波形蛋白的上調和E-cadherin的下調(圖5d,e)。此外,YBX1的敲除至少部分阻斷了769-P細胞中MILIP介導的遷移和侵襲增加(圖5f,g)。總之,這些結果表明MILIP促進YBX1與Snai1 mRNA的結合,并促進YBX1介導的Snai1的翻譯激活。
結論:
TFAP2C響應的MILIP通過與Snai1 mRNA形成RNA-RNA雙鏈以促進YBX1介導的Snai1翻譯激活,促進ccRCC轉移。MILIP在轉移性ccRCCs中上調,且MILIP高表達與ccRCC患者預后不良相關。這些發現揭示了lncRNA介導的促進ccRCC轉移的機制,并暗示靶向MILIP代表了治療晚期ccRCC的新途徑。
參考文獻:
Wang Y, Feng YC, Gan Y, Teng L, Wang L, La T, Wang P, Gu Y, Yan L, Li N, Zhang L, Wang L, Thorne RF, Zhang XD, Cao H, Shao FM. LncRNA MILIP links YBX1 to translational activation of Snai1 and promotes metastasis in clear cell renal cell carcinoma. J Exp Clin Cancer Res. 2022 Aug 26;41(1):260. doi: 10.1186/s13046-022-02452-9.






