P300/SP1復合體/METTL1/m7G/CDK14軸調控去勢抵抗性前列腺癌
m7G修飾是除m6A修飾外更常見的一種表觀遺傳修飾。研究發現m7G修飾在mRNA轉錄、tRNA穩定性、rRNA加工成熟和miRNA生物合成等方面發揮著重要作用。然而, METTL1在腫瘤,特別是前列腺癌(PCa)中的作用尚未被揭示。在這里,我們發現METTL1在去勢抵抗性前列腺癌(CRPC)中升高,并且METTL1升高的患者往往預后較差。功能上,在CRPC細胞中,METTL1的敲低顯著限制了細胞的增殖和侵襲能力。在機制上,我們發現P300可以與SP1形成復合物,并通過SP1結合到METTL1基因的啟動子區域,從而介導CRPC中METTL1的轉錄上調。隨后,我們的研究結果表明,METTL1通過在其mRNA中添加m7G修飾,從而增強CDK14 mRNA的穩定性,最終促進CRPC的進展。本文于2023年8月發表于“Journal of Experimental & Clinical Cancer Research”(IF=11.3)上。
技術路線

結果
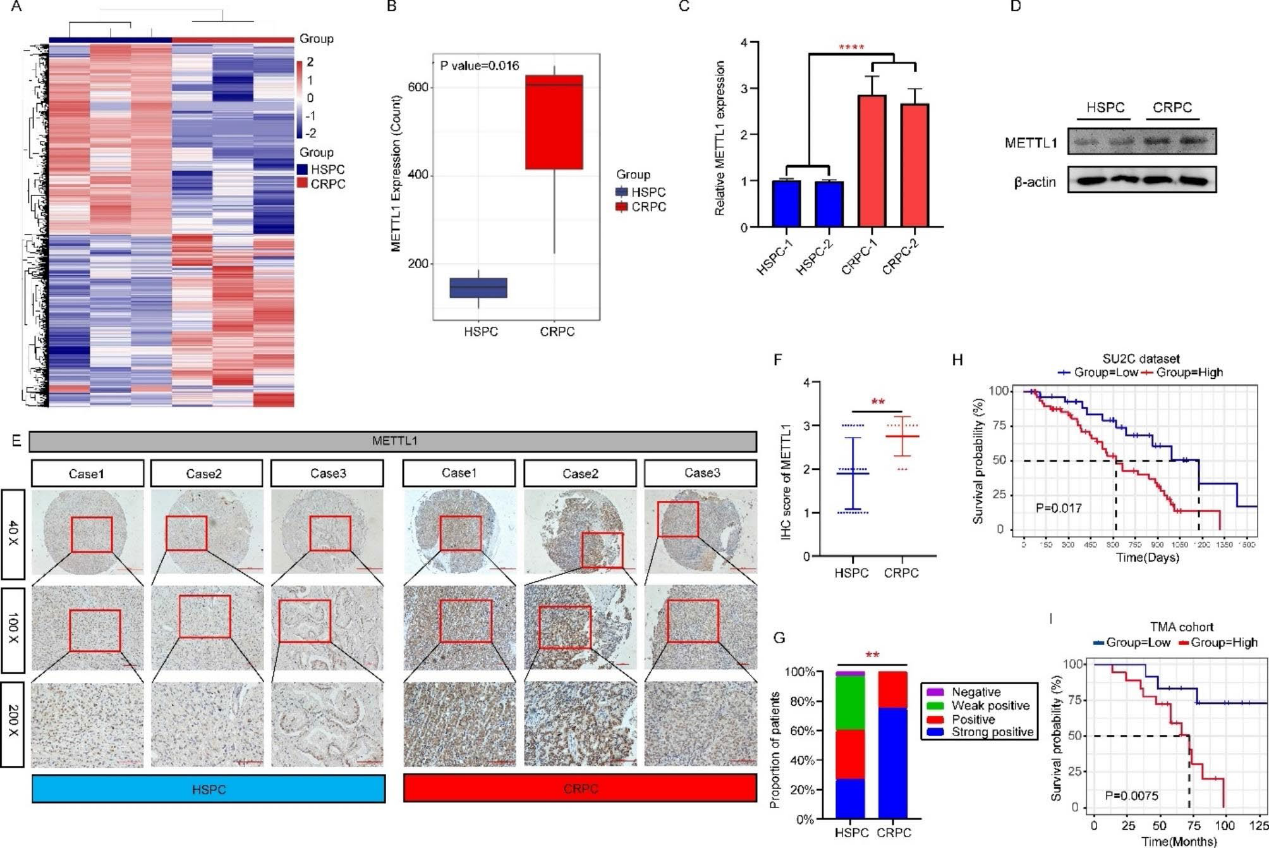
1)METTL1表達升高與CRPC患者預后不良相關
我們對3例CRPC和3例HSPC患者的腫瘤組織樣本進行了全轉錄組測序。根據|Fold change| > 2和p值< 0.05的標準篩選差異表達基因,并以熱圖的形式顯示差異表達基因(圖1A)。根據差異基因的結果,我們發現與HSPC相比,CRPC中METTL1的表達異常升高(圖1B)。為了驗證測序結果的準確性,我們從HSPC和CRPC患者中獲得腫瘤組織,提取mRNA和蛋白,分別檢測METTL1在mRNA和蛋白水平上的差異表達。結果顯示,與HSPC患者相比,METTL1在CRPC患者中的表達水平更高(圖1C和1D)。免疫組化染色實驗發現METTL1在CRPC中的總體表達水平更高(圖1E和1F)。免疫組化染色“陽性”和“強陽性”的患者比例在CRPC中明顯高于HSPC患者(圖1G)。METTL1高表達的CRPC患者生存率較差(圖1H)。根據患者的生存過渡和生存時間,我們還發現METTL1高表達組患者生存和預后較差(圖1I)。綜上所述,我們得出結論,METTL1在CRPC中表達異常上調,且METTL1高表達的患者生存率較差。
2)敲低METTL1抑制CRPC細胞的增殖和侵襲
為了闡明METTL1對CRPC惡性生物學行為的影響,我們在前列腺癌細胞系中進行了表型實驗。我們首先檢測了HSPC和CRPC細胞系之間METTL1水平的差異,發現與HSPC細胞系LNCaP相比,CRPC細胞系中METTL1水平的升高存在差異,其中以LNCaP- ai和C4-2最為突出(圖2A和2B)。隨后,我們以LNCaP- ai和C4-2細胞為研究載體構建了METTL1穩定沉默的細胞系(圖2C-2E)。為了研究METTL1對CRPC細胞增殖能力的影響,我們進行了MTT實驗和克隆形成實驗。結果表明,敲低METTL1降低了細胞的增殖能力,減少了克隆集落形成的數量,并顯著抑制了細胞的增殖能力(圖2F-2K)。最后,我們在LNCaP-AI細胞和C4-2細胞中進行transwell實驗,發現抑制METTL1的表達抑制了細胞的侵襲能力(圖2L-2O)。綜上所述,我們初步得出結論,METTL1的表達與CRPC細胞不良的生物學行為有關。限制METTL1的表達明顯限制了細胞的增殖和侵襲能力。

3)P300的增加通過H3K27乙酰化修飾介導METTL1的高表達
為了探索CRPC中METTL1高表達的潛在分子機制,我們首先通過UCSC在線網站可視化了METTL1基因啟動子的修飾形式。我們在METTL1基因的啟動子區域發現了大量的組蛋白乙酰化修飾峰(H3K27ac),這表明METTL1可能通過染色質乙酰化進行調節(圖3A)。接下來,我們用H3K27ac抗體進行染色質免疫沉淀實驗,發現在LNCaP- AI和C4-2細胞中,METTL1啟動子區H3K27ac修飾的豐富度高于LNCaP細胞(圖3B)。這表明CRPC中METTL1水平的異常上調可能與METTL1基因啟動子區H3K27ac的高修飾有關。考慮到P300是介導H3K27乙酰化修飾的關鍵酶,我們用P300抑制劑C646處理LNCaP-AI和C4-2細胞,發現用20 μM濃度的C646處理細胞48 h后,METTL1 mRNA表達顯著下降(圖3C和3D)。隨后,我們用不同濃度梯度的C646處理細胞,在48 h時間點,我們發現,當C646濃度為20 μM時,METTL1 mRNA水平的下降最為明顯(圖3E和3F)。隨后,我們還證實,在P300抑制劑C646 (20 μM,48 h)處理后,組蛋白H3K27ac和METTL1在蛋白質水平上都有所下降(圖3G)。接下來,我們使用組織微陣列進行染色分析,發現P300和METTL1之間呈正相關(圖3H和3I)。此外,我們設計了siRNA來抑制P300的表達(圖3J),并證實P300的敲低可以抑制METTL1的表達(圖3K和3L)。為了進一步證明P300的敲低導致METTL1 mRNA水平的降低是由于METTL1啟動子區域H3K27ac水平的降低引起的,我們進行了染色質免疫沉淀實驗。結果表明,P300的抑制也顯著降低了METTL1基因啟動子區域的H3K27ac水平(圖3M和3N)。上述實驗結果初步證明P300介導的METTL1啟動子區H3K27ac的修飾是導致CRPC中METTL1 mRNA的上調的一個重要的機制。

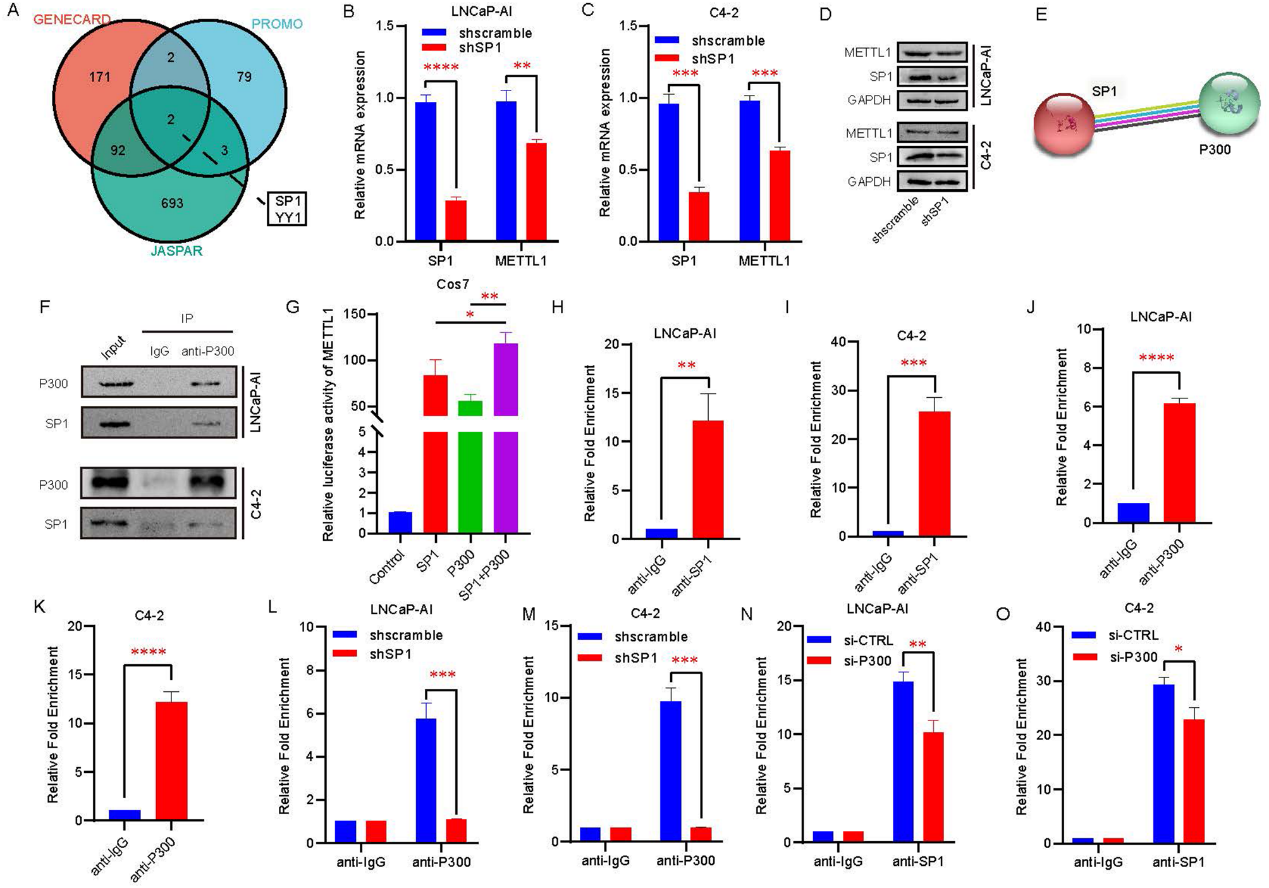
4)P300/SP1復合體調節METTL1的轉錄活性
為了進一步研究導致METTL1轉錄上調的分子機制,我們首先通過GENECARD、PROMO和JASPAR網站預測了METTL1的潛在轉錄因子。三個數據庫發現SP1和YY1是共享的(圖4A)。鑒于SP1在前列腺癌關鍵基因轉錄調控中的重要作用,我們構建了LNCaP-AI和C4-2中SP1穩定敲低的細胞系,發現SP1的沉默降低了METTL1的表達水平(圖4B-4D)。P300作為一種重要的轉錄共激活因子,除了具有乙酰轉移酶活性外,還經常通過不同的作用方式參與基因的轉錄調控。在這里,我們通過生物信息學手段預測SP1和P300可能相互作用(圖4E)。隨后,我們通過免疫沉淀實驗證實了相互結合的存在(圖4F)。接下來,我們在COS7細胞中通過熒光素酶報告基因實驗驗證,當SP1和P300同時存在時,METTL1的轉錄活性比它們單獨存在時更強(圖4G)。為了闡明SP1和P300復合物與METTL1啟動子區域結合的方式,進行了一系列CHIP-qPCR實驗。我們一方面發現SP1和P300可以直接或間接結合到METTL1啟動子區域(圖4H-4K),另一方面,我們發現在沉默SP1后,P300幾乎不再結合到METTL1啟動子區域(圖4L和4M)。然而,在抑制P300后,SP1與METTL1啟動子區域的結合減少,但結合仍然存在(圖4N和4O)。這些結果表明,轉錄因子SP1能夠與P300形成復合物介導METTL1的轉錄激活,并且SP1而不是P300可以直接結合到METTL1啟動子區域啟動轉錄。
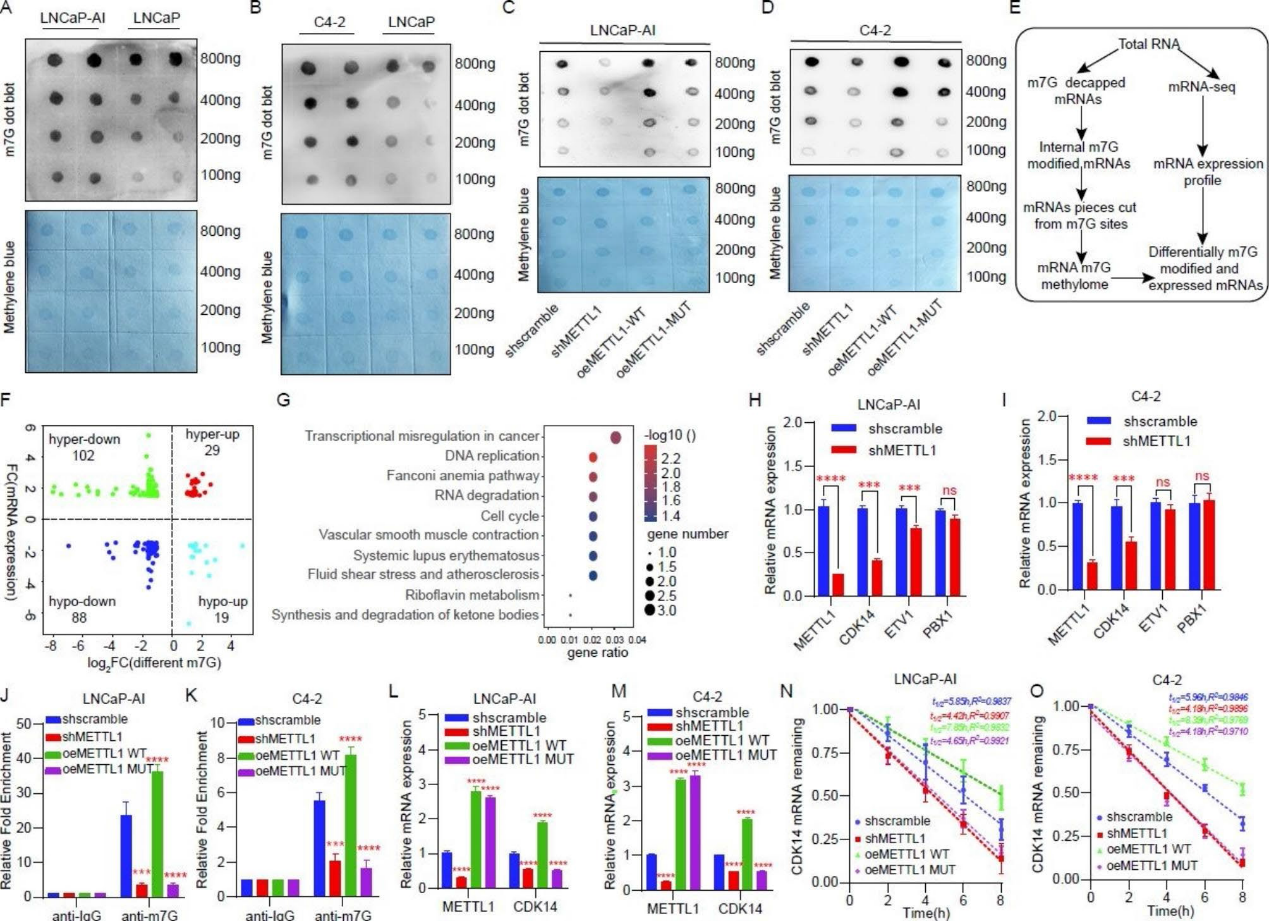
5)METTL1通過介導內部m7G修飾來穩定CDK14 mRNA
為了進一步探討METTL1影響CRPC細胞系增殖和侵襲能力的分子機制,我們首先驗證了其在CRPC中的生物學功能。考慮到METTL1是一種甲基轉移酶,負責催化m7G修飾。我們檢測了HSPC和CRPC細胞mRNA中m7G水平的差異。在用decapping酶處理細胞后,我們發現LNCaP-AI和C4-2細胞的mRNA中m7G修飾水平比LNCaP細胞更豐富(圖5A和5B)。接下來,我們構建了METTL1野生型和酶活性突變型過表達質粒。我們發現,METTL1沉默后,CRPC細胞mRNA中的m7G水平顯著降低,轉染METTL1野生型過表達質粒后,mRNA中的m7G水平恢復,但轉染METTL1酶活性突變質粒后,細胞中的m7G水平未見增加(圖5C和5D)。這些結果表明,mRNA中的m7G修飾是由METTL1催化的。為了進一步闡明METTL1催化的mRNA內m7G修飾的生物學作用,我們進行了RNA-seq和mRNA內m7G AlkAniline-Seq聯合分析(圖5E和5F)。然后,我們對敲低METTL1導致mRNA和m7G水平下調的基因進行了功能富集分析,發現這些基因主要富集在癌癥等通路的轉錄失調中(圖5G)。然后我們驗證了該通路中CDK14受METTL1調控最為顯著(圖5H和圖5I)。為了弄清楚并證實METTL1對CDK14的調控依賴于甲基轉移酶活性,我們一方面通過MeRIP-qPCR闡述了沉默METTL1后CDK14 mRNA內m7G水平下降,轉染METTL1野生型質粒后m7G水平升高;而轉染突變METTL1質粒后,m7G水平沒有明顯改變(圖5J和5K)。另一方面,CDK14 mRNA水平與其m7G水平的變化一致(圖5L和5M)。為了更深入地探討mRNA內CDK14 mRNA和m7G水平變化一致的原因,我們進行了RNA降解試驗。實驗結果表明,METTL1的沉默導致CDK14 mRNA半衰期縮短。METTL1野生型質粒的過表達延長了CDK14 mRNA的半衰期,而突變型METTL1質粒的過表達對CDK14 mRNA的半衰期沒有顯著變化(圖5N和圖5O)。這些結果表明,甲基轉移酶METTL1通過在CDK14 mRNA內引起m7G修飾來保護CDK14 mRNA免受降解。
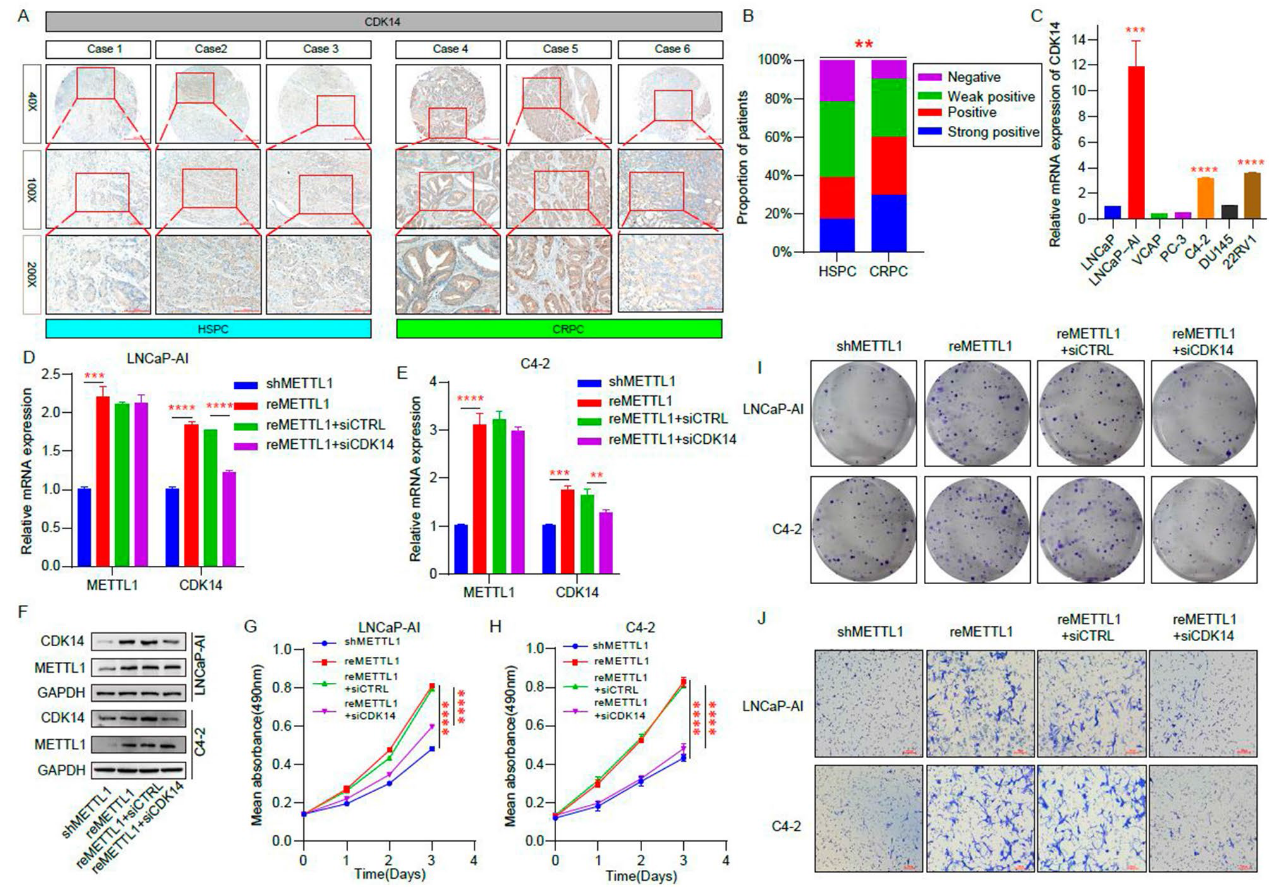
6)METTL1通過調節CDK14的表達調控CRPC的增殖和侵襲
為了進一步證實METTL1通過調節CDK14的表達對CRPC惡性生物學的影響,我們首先檢測了CDK14在HSPC和CRPC組織中的表達,免疫組化染色結果顯示,與HSPC患者相比,CRPC中CDK14的表達水平更高(圖6A和6B)。此外,我們還發現CDK14在LNCaP-AI、C4-2和22RV1中顯著上調(圖6C)。然后,我們在穩定敲除METTL1 (shMETTL1)的細胞中過表達METTL1 (reMETTL1),同時使用siRNA (reMETTL1 + siCDK14)抑制CDK14的表達,并比較不同組之間增殖和侵襲能力的差異(圖6D-6F)。MTT和克隆形成實驗表明,與敲低METTL1組相比,過表達METTL1后細胞增殖增強,然而,在此基礎上抑制CDK14表達降低了細胞增殖(圖6G – 6I)。同樣,transwell實驗顯示,過表達METTL1后,CRPC細胞的侵襲能力增強,而抑制CDK14表達則使CRPC細胞的侵襲能力受損(圖6J)。以上結果表明,METTL1可以通過CDK14間接調節CRPC細胞的增殖和侵襲能力。
7)METTL1在體內促進CRPC的進展
為了確定METTL1在體內促進CRPC進展中的作用,我們使用免疫缺陷裸鼠進行皮下移植腫瘤實驗。結果表明,與對照組相比,敲除METTL1組皮下移植腫瘤生長更慢,最終體積和質量更小。對照組裸鼠皮下移植瘤生長速度最快,體積和重量最大。同時,CTPB + shMETTL1組比DMSO+shMETTL1組生長更快,腫瘤體積和質量更大(圖7A-7C)。通過免疫組化染色,我們發現METTL1抑制后CDK14和細胞增殖標志物PCNA均減少。與sh-scramble和shMETTL1組相比,CTPB飼養的裸鼠中CDK14和PCNA表達升高(圖7D和7E)。體內實驗更嚴格地證實了METTL1在促進CRPC進展中的重要作用。

結論
METTL1在CRPC的進展中起致瘤作用。從機制上講,P300/SP1復合體促進了METTL1的轉錄激活,導致METTL1在CRPC中異常高表達。最后,作為m7G甲基轉移酶,METTL1通過在其內部添加m7G修飾來保護CDK14 mRNA免受降解并最終導致CRPC進展。
實驗方法
TMA,IHC,WB,RT-qPCR,MTT,克隆形成實驗,transwell,m7G點印跡,Co-IP,CHIP,熒光素酶報告試驗,MeRIP,mRNA穩定性實驗,體內實驗。
參考文獻
Zhang M, Kan D, Zhang B, Chen X, Wang C, Chen S, Gao W, Yang Z, Li Y, Chen Y, Zhu S, Wen S, Niu Y, Shang Z. P300/SP1 complex mediating elevated METTL1 regulates CDK14 mRNA stability via internal m7G modification in CRPC. J Exp Clin Cancer Res. 2023 Aug 21;42(1):215. doi: 10.1186/s13046-023-02777-z.






